Mozak u posudi je koncept koji predstavlja budućnost. Sve što nas čini ljudima nalazi se unutar 1,4 kilograma žućkastog tkiva koje gradi mozak čoveka. Pomoću njega mislimo, volimo, mrzimo. On je mesto gde se stvaraju najkreativnije i najzločestije ideje ljudskog roda. Ova struktura orašastog oblika je i najkompleksniji organ koji je priroda stvorila. Mozak je utočište za 86 milijardni neurona, koji moraju biti rođeni u pravo vreme, koji moraju da migriraju na pravo mesto i da se međusobno povežu na ispravan način, tako prežive i napreduju. Potpuno razumevanje načina na koji se ljudski mozak razvija i funkcioniše je najveći izazov moderne biologije. Do sada najviše saznanja o mozgu dobijeno je iz eksprimenata na miševima i pacovima. Ispitivanja na ovim životinjama su vršena jer njihov mozak i ljudski istoimeni organ imaju sličnu arhitektoniku: poseduju mnoge iste vrste nervnih ćelija, koriste iste delove mozga za mentalne procese. Ali ljudi i glodari se razlikuju u jednoj ključnoj stvari, mozak glodara ima glatku površinu dok ljudski mozak ima useke i vijuge. Tako da površina ljudskog mozga nije zaravnjena.
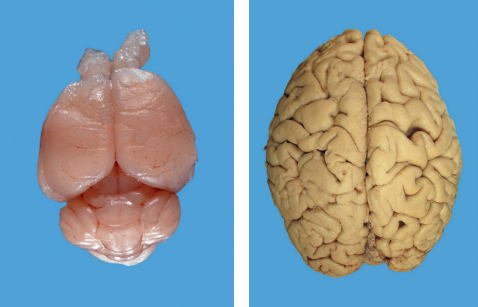
Foto Credit: Treuting M. P., Dintzis M. S. Comparative anatomy and histology a mouse and human atlas, First edition, Elsevier, 2012. – Mozak u posudi –
Neurobiolozi veruju da ljudski mozak u odnosu na glodare funkcioniše drukčije zbog njegove nabrane površine. Ovakva arhitektonika omogućava postojanje većeg broj neurona u kori, sadrži i istaknute odlike svih „inteligentnih“ životinja poput majmuna, mačaka, pasa i kitova. Evolucioni biolozi su dokazali da nabrana površina potiče od još jedne razlike između mozga miševa i ljudi: neuroni u mnogim delovima mozga potiču od specifičnih prekursornih ćelija koji kod miševa postoje samo tokom nekoliko minuta, dok kod ljudi dosta duže. Ovakva razlika je moguće objašnjenje zašto mnoge genetičke mutacije koje uzorkuju teške neurološke poremećaje kod ljudi gotovo nikako ne deluju kod miševa tokom eksperimenata. Eksperimentisanjem na glodarima naučnici su ispitivali mehanizam bolesti koje postoje kod ljudi. Jedinstvena građa ljudskog mozga može biti jedan od razloga zašto dosadašnje studije na glodarima nisu otkrile adekvatnu terapiju za šizofreniju, epilepsiju i autizam.
Prepoznavanje razlike između mozga čoveka i glodara podstakla je potragu za određenim i efikasnijim načinom za izvođenje eksperimenata. Tako je nastalo jedno izvanredno otkriće. Naučnici su usepli da u laboratoriji uzgoje deo mozga u razvoju (mozak u petrijevoj šolji). Ove mozgolike strukture se zovu organoidi. Oni predstavljaju model ljudskog mozga na kome naučnici izvode studije koje nisu održive na miševima. Istraživači mogu da nadgledaju šta se dešava kada je „mozak u posudi“ ili mini mozak izložen naprimer Zika virusu. Ovaj virus je specifičan jer ometa razvoj mozga u fetusu kod inficiranih žena. Takođe promene mogu da posmatraju kada je organoid genetski programiran da oponaša bolestan mozak.
Mozak u posudi
Naučnik Jirgen Knoblik (eng. Juergen A. Knoblich – zvanje: Senior scientist and deputyscientific director of the Institute of Molecular Biotechnology of the Austrian Academy of Sciences u Beču) bavi se proučavanjem nervnih matičnih ćelija i razvoja nervnog sistema voćne mušice. Njegova laboratorija počela je da radi sa organoidima 2012. godine. Tada je Medlin Lankaster (eng. Madeline A. Lancaster) u to vreme na postdoktorskim studijama u laboratoriji dr Jirgena smislila kako da matične ćelije transformiše u tkivo mozga koje je veliko kao mozak fetusa u desetoj gestacionoj nedelji. Matične ćelije koje su okosnica otkrića imaju izuzetnu osobinu koja se zove pluripotentnost. Pluripotentne matične ćelije su iste kao i one koje se nalaze u ranom razvoju embriona. Kada se uzgajaju pod odgovarajućim uslovima transforimišu se u bilo koju vrstu tkiva nervno, mišićno, koštano, krv i sl. Kod fetusa ove ćelije zadržavaju pluripotentnost samo nekoliko dana. Koristeći specijalizovane laboratorijske postpuke i podloge naučnici su uspeli da te ćelije održavaju u pluripotentnom stanju neograničen vremenski period i da ih na kraju pretvore u bilo koje željeno tkivo.
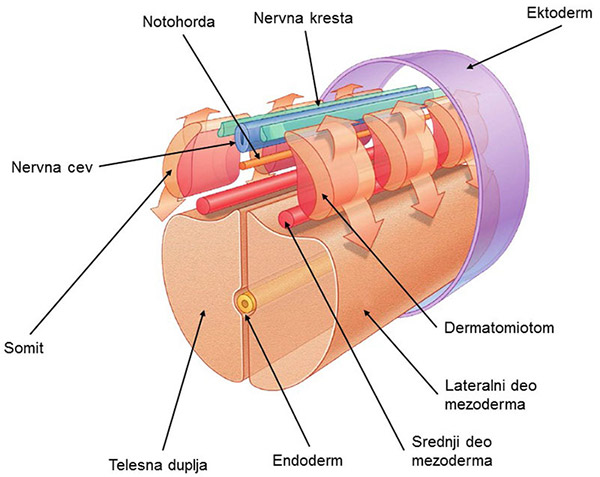
Foto Credit: Drake L. R., Vogl A. W., Mitchell W. M. A. Grey’s anatomy for students, Second edition, Elsevier, 2010.
Nastanak novog tkiva
Na početku kultura ćelija se stavi u tečnu podlogu koja sadrži sve potrebne nutritijente za rast neuroektoderma (Slika 2). Kada se ćelije grupišu u loptu zvanu embrionsko telo stavljaju se u Matrigel. Ovaj gel se sintetiše iz kulture ćelija izolovanih iz tumora hrskavice kod miševa. Gel je sličan membrani na kojoj se nalaze ćelije u fetusu. Matrigel osim što je bogat supstancama koje stimulišu deobu ćelija i čuvaju ih od umiranja, obezbeđuje kostur koji je dovoljno uzan da drži ćelije zbijene ali je takođe elastičan i savitljiv da se prilagođava broju ćelija i tako menja oblik. Ishod ovog eksperimentisanja je neverovatan. U gelu embrioidna tela rastu u trodimenzionalan oblik. To su bele lopte tkiva koja su slična mozgu ljudskog embriona. Izloženi dejstvu odgovarajućih hemijskih signala koji pokreću razvoj fetalnog mozga, matične ćelije rastu u preciznu repliku čovečijeg prednjeg mozga, region koji je zadužen za više mentalne funkcije. Prednji mozak čine komponente poput korteksa i horoidnog pleksusa.
Ćelije oraganoida – Mozak u posudi – u razvoju raspoređuju se identično kao u mozgu fetusa tokom osme, devete i desete nedelje intrauterinog razvoja. U retkim slučajevima na organoidima se razviju male očne duplje, udubljenja u tkivu koje sadrži pigment u boji, slično kao kod početka formiranja ljudskog oka. U organoidu ćelije se dele u različite vrste nervnih ćelija, kao i kod fetusa. Nuroni stvaraju aksone koji ih spajaju sa drugim neuronima i tako stvaraju mrežu za prenos impulsa odnosno za međusobnu komunikaciju. Pre nego što kreiraju ovu mrežu, neuroni migriraju sa jednog mesta na drugo kao što rade kod fetusa, što može dati uvid u to šta se dešava kada neuroni završe na pogrešnom mestu kao što se često dešava kod psihijatrijskih bolesti. Za sada mozak u posudi koncept ima i mane.
Kako je nastala ideja za ovaj poduhvat
Ideja o proizvodnji tkiva nije sasvim nova. Napredovanjem tehnologije ona se samo usavršavala. Već 1907. godine zoolog Henri Vilson (eng. Henry Wilson) demonstrirao je da niži organizmi poput sunđera mogu ponovo da izrastu ako se razbiju na jednu ćeliju. Godine 1939. Johanes Holtfreter (eng. Johannes Holtfreter) otkrio je da različite ćelije embriona žabe „traže“ jedna drugu i regenerišu svoj oblik čak i onda kada su kompletno razdvojene. Tokom osamedesetih godina prošlog veka ova otkrića dovela su do velikog napretka i unapređivanja ispitivanja tako da su kompleksni životinjski organi poput retine pa čak i moždanog korteksa stvoreni u laboratoriji spajanjem njihovih različitih ćelijskih tipova.
Slična ispitivanja tokom perioda 2006. do 2010. godine sprovodio je i japanski naučnik Jošiki Sasaji (eng. Yoshiki Sasai) u Riken centru (eng. RIKEN, Center for Developmental Biology). On je pionir u oblasti korišćenja matičnih ćelija. Od njih je uzgajao tkivo nervnog sistema, pre svega retinu čoveka. Zapravo mozgoliki organoidi su spoj ove tehnologije i revolucionarne tehnike naučnika Hans Kleversa (eng. Hans Clevers) sa Utreč Unverziteta u Holandiji (eng. Utrecht University). Hans je matične ćelije stavljao u Matrigel kako bi kreirao kulturu koja bi koristila za uzgajanje creva, želuca, čak i jetre i pankreasa.
Tehnologija razvoja Organoida doktora Jirgena prilično je uzdrmala područije biomedicinskog istraživanja. Takozvano reprogramiranje je izumeo japanski naučnik i dobitnik Nobelove nagrade Šinja Jamanaka (eng. Shinya Yamanaka) sa Univerziteta u Kjotou (eng. Kyoto University). Kroz jednostavan postupak genetske manipulacije, gde reprogramiranjem pretvara sazrele telesne ćelije u pluripotentne matične ćelije. Ovom postupku mogu se podvrgnuti sve ćelije od ćelija kože do krvnih ćelija. Matične ćelije nastale iz ćelija kože ili krvi mogu biti transformisane u različit tip ćelija mozga, i takve ćelije mogu se razvijati u organoide. Na ovaj način nisu potrebne embrionalne ćelije. Reprogramiranje omogućava uzgajanje organoida od ćelija pacijenta koji boluje od neke genetske bolesti, i poređenje sa organoidom od zdrave osobe. Ovako se može uočiti razlika i potencijalan uzrok bolesti jer genetski defekt izaziva bolest na organoidu kao što izaziva bolest na fetusu u razvoju.
Zapravo, model organoida – mozak u posudi je već korišćen kako bi se dobio uvid kod mikrocefalije u pacijenata koji su rođeni sa veoma smanjenom veličinom mozga. Istraživači su otkrili da su organoidi uzgajani od ćelija pacijenata sa mikrocefalijom znatno manji. Zbog mogućnosti uzgoja neograničenog broja ćelija pacijenata naučnici mogu da analiziraju lanac molekularnih zbivanja koji dovodi do mikrocefalije kod fetusa. Postupak bi trebalo da važi za sve bolesti mozga: koristeći ćelije pacijenata za uzgoj organoida neurolozi će bolje razumeti poremećaje u mozgu koji dovode do šizofrenije, epilepsije i druge bolesti koje se teško ili nikako ne mogu proučavati na životinjama.
Organoidi – mozak u posudi – nastali od reprogramiranih ćelija zdravih osoba takođe mogu biti korisni. Oni su već našli svoju upotrebu tokom epidemije Zika virusa koji izaziva mikrocefaliju u beba čije su majke inficirane ovim virusom tokom trudnoće. Mnoge laboratorije rade sa organoidima prvo u Brazilu, a potom u SAD. U njima su naučnici otkrili da Zika virus izaziva mikrocefalju pomoću modela organoida. Kada se organoid zarazi Zikom nervne ćelije odumiru što dovodi do znatnog smanjenja veličine organoida u odnosu na nezaražene. Pretpostavlja se da će organoidi pomoći i kod ostalih istraživanja Zika virusa. Jedan način je da nekoliko organoida bude zaraženo različitim sojevima pomenutog virusa iz različitih delova sveta, da bi naučnici shvatili zašto virus dovodi do mikrocefalije u jednoj oblasti ali ne i u drugoj. Istraživači takođe mogu da ispitaju zašto kod nekih pojedinaca dolazi do nastanka mikrocefalije posle inficiranja virusom. Ili da na modelu organoida pokušaju da otkriju receptor koji virus koristi za ulazak u ćeliju, što može biti izuzetno važno za ispitivanje potencijalnih antivirotika pre kliničkog ispitivanja na pacijentima.
Istraživači mogu koristiti organoide – mozak u posudi – kako bi menjali njihov genetski kod. U genom organoida se ubaci mutacija za koju se sumnja da dovodi do neke bolesti. Ovako naučnici mogu utvrditi da li će defekt izazvati bolest. Ispravljanjem mutacije ispitivači mogu proceniti da li će organoid biti zdrav. Ovaj put može voditi ka novim tretmanima za popravljanje genetskih mutacija.
Neurolozi su željni da istraže i druge primene ove „mozak u malom“ tehnologije, kao što je razvoj lekova. Pomoću ove tehnologije može se proceniti da li novi lekovi ispoljavaju željeno dejstvo na mozak izbegavajući ispitivanja na životinjama, tako dolazi i do smanjivanja troškova razvoja samog leka. Na organoidima – mozak u posudi – se takođe mogu otkriti neželjeni efekti koji se mogu javiti kod mozga fetusa tokom intrauterinog razvoja. „Mini mozgovi“ su postali neprocenjiva alatka za evolutivne biologe. Može se koristiti za identifikovanje gena odgovornih za ogromnu veličinu ljudskog mozga u odnosu na ostale primate. Poređenjem genoma ljudi i primata već su identifikovani geni koji bi mogli biti odgovorni za kognitivne funkcije kao što su jezik, koji je samo jedinstven za ljude.
Da li treba da se plašimo?
Organoidi nisu funkcionalni mozgovi, već samo nakupina tkiva koja imitira molekularnu i ćelijsku funkciju organa (mozga) veoma detaljno. Oni su jako slični delovima tkiva koji su uklonjeni tokom operacije na mozgu, nisu svesna bića. Ipak, uzgajanje organoidi povlači za sobom određene etička i legalna pitanja. Postupanje sa organoidima koji potiču od ćelija pacijenta podleže određenim pravilima. Pacijent mora da da saglasnost pre nego što se njegove ćelije iskoriste za istraživanje. Takođe laboratorija u kojoj se izvode ovakvi postupci mora imati odgovarajuća odobrenja.
Budućnost tehnologije – Mozak u posudi
Benefiti ove tehnologije su izvanredni. Na moždanim organoidima od ljudskog tkiva mogu se izvoditi toksikološka i razna druga ispitivanja, te nema potrebe za testiranjem na životinjama. Međutim potrebno je „mini mozgove“ unaprediti. Najnovijoj generaciji nedostaju krvni sudovi. Tokom faze ranog razvoja organoida oni nisu potrebni, ali vremenom ćelije umiru zbog nedostatka kiseonika i nutritijenata. U teoriji moguće je napraviti krvne sudove uz pomoć štampanja 3D modela ili razviti ih od matičnih ćelija. Još jedan nedostatak je to što organoidi nemaju orjentacione ravni. Kao takvi rastu bez pravila, tako da njihovi delovi imaju različite orjentacije. Tokom fetalnog razvoja mozga kompleksan sistem hemijskih signala omogućava uobičajen razvoj mozga, tako da se njegovi delovi nalaze u odgovarajućim ravnima. Naučnici se nadaju da će pomenute hemijske molekule iskoristiti i kod organoida. Kao rezultat trebalo bi da se razviju organoidi sa prednjim mozgom napred i malim mozgom na suprotnoj strani. Na razvoju organoida naučnici rade veoma naporno, a u budućnosti nam se spremaju nova iznenađenja i otkrića jer možda jednog dana uspeju da nađu lek za šizofreniju, autizam i mnoge druge mentalne bolesti.
Literatura korišćena za tekst Mozak u posudi je:
- Scientific American – January 2017.
- Treuting M. P., Dintzis M. S. Comparative anatomy and histology a mouse and human atlas, First edition, Elsevier, 2012.
- Drake L. R., Vogl A. W., Mitchell W. M. A. Grey’s anatomy for students, Second edition, Elsevier, 2010.